第二节 酶活性测定的常用技术和方法
从广义上说,任何一种可以测定反应物变化速度的分析技术,不论是经典的比色法、容量法,还是现代的仪器分析技术都可用来测定酶活性浓度,但从历史和发展来看,主要还是使用分光亮度法和量气法。
一、量气法
在封闭的反应系统中如有气体变化,通过测量变化后的气体体积或压力很容易计算出气体变化量,这是量气法的基本原理。曾在检验科广泛应用的Van-slyke测二氧化碳结合力的方法就是量气法的一个典型例子。Warburg进一步加以发展,设计出专用于测定酶活性的华勃呼吸仪。这种仪器特别适用于测定那些在反应中产生或消耗气体的酶,例如氧化酶反应涉及到O2的消耗,脱羧酶会产生CO2。但也不仅限于这些酶,科学家采用与CO2气体保持平衡过的重碳酸盐体系,可用来测定各种产生H+的酶反应,如各种还原酶,可使NADH变为NAD和H+,而H+会促使反应体系中重碳酸盐变为CO2气体。
二、比色法与分光亮度法
在20世纪上半个世纪华勃仪得到研究实验室广泛的应用,并在酶学上得到丰硕的成果。但此法操作烦琐,技术要求高而且灵敏度低。临床常规中很少使用。多使用简单易行的比色法测酶活性。在上半个世纪建立了一些适用于常规工作的测酶活性浓度的方法,如测定淀粉酶的Somogyi法,碱性磷酸酶的Bodansky法、King法等等。这些方法都是在酶和底物作用一段时间后停止酶反应,加入各种化学试剂与产物或基质反应呈色,用比色计在可见光处比色,同时将被测物质作标准管或标准曲线,比较后计算出在此段时间内产物生成量或底物消耗量,从而求得反应速率v。
比色法从50年代起逐步被分光光度法所取代。这是因为分光光度法有以下几个显著优点:一是测定范围不只局限在可见光,还可扩展到紫外和红外部分。这就为扩大测定酶范围提供了可能性。二是提供了寻找一类不需停止酶反应就可直接测定产物生成量或底物消耗量方法的可能性。例某一酶催化下列反应A->B+C,A、B、C三种物质用分光光度法的吸收光谱如图17-1所示。
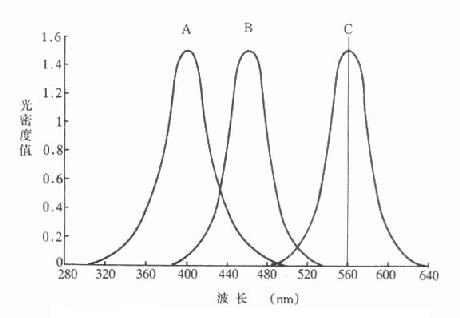
图17-1 A、B、C三种物质的吸收曲线
可以看到C在560nm处有一吸收峰,而A和B在此处无吸光度变化因此无需停止酶反应,只要在560nm处测定吸光度变化就很容易计算出C的变化速度,而且C物质比A、B二物质有更高的吸收峰,即灵敏度最高。
这类方法中最成功的是Warburg在50年代利用NAD(P)H和NAD(P)吸收光谱差异建立的测酶活性浓度方法。NAD(P)H在340nm处有一吸收峰,而NAD(P)在此波段却毫无吸光性。因此建立了一类和原来比色法截然不同方法。不需停止酶反应,在340nm根据吸光度变化,就可观察到酶反应变化全过程。
第三个优点是不需要如比色法那样,作标准管或标准曲线,因为分光光度计使用近似单色光的光源,在此条件下,某一特定物质的吸光度为常数,即人们所熟悉的摩尔吸光度(molar absorbance)。根据此值从吸光度△A/△T不难计算出酶催化反应速度v。
分光光度计的这些简便、准确等特点使它在近年来已逐步取代比色法而成为目前最流行的方法。其缺点是需要精确带恒温装置的分光光度计,在经济不发达地区尚难推广。
分光光度法的技术多样化。设计得当可用于各种酶的测定。表17-2是一些可用于分光光度法的氧化还原物质特性。
除了前述的NAD(P)H系统可用于脱氢酶测定外,可利用黄素单核苷酸(FMN)和黄素腺嘌呤二核苷酸(FAD)来测定各种含这二个辅基的酶。它们的氧化型在450nm有一很强吸收峰,而还原型的吸光度很低,同样细胞色素还原型在可见光有一个非常明显和很窄的吸收峰,都使人们很容易用分光光度法研究这些酶的作用。上述物质主要用于氧化还原酶的测定。
科学家还设计出一系列人工合成酶的底物,用于其它酶的分光光度法测定。例如合成了很多对硝基酚的衍生物,用于各种水解酶的测定。碱性磷酸酶底物磷酸对硝基酚就是一个成功例子。又如测芳香基硫酸酯酶,可使用人工合成的硫酸对硝基酚为底物,其分解产物的吸收峰由原来的278nm变为318nm,Webb成功地在330nm进行此酶监测。
表17-2 一些氧化还原物质的特性
| 物质 | 波长(nm) | 克分子吸光度 | |
| 还原型 | 氧化型 | ||
| NAD,NADP | 340 | 6300 | 0 |
| FMN | 450 | 12200 | |
| FAD | 450 | 11300 | |
| 细胞色素C | 550 | 29500 | 8300 |
| 亚甲蓝(等消光点) | 610 | 0 | 41000 |
| 二氢酚吲哚酚 | 600 | 0 | 21000 |
| 吩嗪甲酯硫酸 | 388 | 1500 | 22000 |
| 抗坏血酸 | 265 | 15100 | |
| 连二亚硫酸盐 | 314 | 8000 | 0 |
| 氰化铁(亚铁) | 420 | 0 | 1020 |
分光光度法的上述原理还可以用于其它酶的测定,如烯醇化酶、延胡索酸水解酶的底物由于含不饱和键,在330nm处有很强吸收峰,而酶作用产物无此不饱和键。则不难在330nm处对这些酶进行直接测定。
此后在分光光度法的发展过程中又导入了酶偶联技术。使得分光光度法几乎能测定所有的酶。因此临床实验室工作者如不能很好掌握分光光度法的技术,不了解各种影响因素,要作好酶的测定是很困难的。
三、荧光法和同位素法
分光亮度法有一个缺点,即灵敏度较低。有些标本中酶浓度很低时往往测不出来。此时可考虑改用荧光法,可将测定灵敏度提高2-3个数量级。如科学家合成了一系列甲基伞形酮的衍生物,可取代对硝基酚衍生物做为一些水解酶的底物,由于水解产物甲基伞形酮有强烈荧光,大大提高测定的灵敏度,就是分光亮度法中最常用的NAD(P)H反应系统,也可改用荧光法,在340nm紫外线激发下NAD(P)H产生强烈的蓝色荧光,而NAD(P)不被激发。此外,还可使用在荧光法基础上发展起来的时间分辨荧光法,例如北京医院就曾利用此种灵敏度极高方法测定很难用其它方法检测的脑脊液中微量的烯醇化酶。荧光法不易掌握,对所用的试剂、容器和仪器都要求很高,否则易产生非特异荧光干扰测定,或者引起荧光的淬灭使测定不准,故此种方法多用于研究实验室,少用于常规实验室。为提高灵敏度,还可使用同位素标记的底物进行酶测定,例如,有人以C12标记的乙酰胆碱为底物测定胆碱酯酶,在酶作用后以离子交换法分离出含C14的乙酸。同位素方法由于对人体有害,操作麻烦,目前已很少使用。
四、其它方法
离子选择电极法,旋光法等有时用于测定特定的酶,当酶反应牵涉到有酸碱变化时,很容易用pH仪直接观察酶反应过程中H+的变化。直接用pH仪测酶反应有两个缺点:一是随pH变化,会偏离酶作用的最适pH值,不可避免地引起酶反应速度变慢。其二是如测定的标本不是纯酶时标本中其他蛋白及其它有缓衡能力的物质将会影响所测pH变化的程度。此时如改用电位滴定仪则更为适合。此仪器可在酶反应过程中不断向反应体系中加入酸或碱以维持反应体系pH的恒定,而加入的酸碱量只与体系中H+变化量相关,和反应体系中缓衡能力无关。
同样如酶反应中有O2变化,可使用氧电极来监测酶反应过程,这可用来测定葡萄糖氧化酶活性,Chappell还成功地将此技术用于测线粒体的氧化能力。还曾有人尝试用二氧化碳和氨电极测酶,由于这些电极反应时间较慢,不利于检测酶反应速度。有些酶的反应物为光学异构体,则可根据旋光度变化来追踪酶反应。某些反应物如羟基酸本身虽无旋光性,但与钼结合后产生很高的旋光性。根据此特性建立了测定延胡索酸水合酶的方法。还有个别酶的测定使用了极谱法、高效液相色谱法等。总之,实验室工作者完全可以根据实验室现有仪器和技术,创造性地建立一些新的测活性浓度的方法。
-
《临床生物化学》 中的相关章节:
……
第三节 离心技术的应用
第四节 层析技术的应用
第五节 电化学分析技术的应用
第十七章 血清酶定量的检测技术
第一节 概述
第二节 酶活性测定的常用技术和方法(当前页)
第三节 酶活性测定条件的选择和限定
第四节 测定酶活性浓度的两大类方法
第十八章 诊断分子生物学基本技术
第一节 概述
……