第三节 脂蛋白受体
脂类在血液中以脂蛋白形式进行运送,并可与细胞膜上存在的特异受体相结合,被摄取进入细胞内进行代谢。迄今为止报道的受体已有很多种,研究最详尽的是LDL受体,其次是清道夫受体,再就是VLDL受体。这三种受体的氨基酸序列、构象及与配体的结合部位都已阐明,并且已成功地得到其cDNA。Brown和Goldstein于1974年研究家族性高胆固醇血症(familialhypercholesterolemia,FH)患者代谢缺陷时,在成纤维细胞膜上发现了LDL受体(LDLreceptor,LDLR)的存在。以后相继发现有VLDL受体和清道夫受体。脂蛋白受体在决定脂类代谢途径、参与脂类代谢、调节血浆脂蛋白水平等方面起重要的作用。脂蛋白受体的发现是脂类代谢研究的里程碑,推动了脂蛋白、载脂蛋白的深入研究。
一、LDL受体
最先从牛肾上腺分离出LDL受体,以后又分离了编码牛LDL受体羟基末端1/3氨基酸的cDNA,并初步阐明了牛LDL受体的cDNA,并且推导出人LDL受体的氨基酸序列。
(一)LDL受体结构
LDL受体是一种多功能蛋白,由836个氨基酸残基组成36面体结构蛋白,分子量约115ku,由五种不同的区域构成,各区域有其独特的功能,见图4-6。
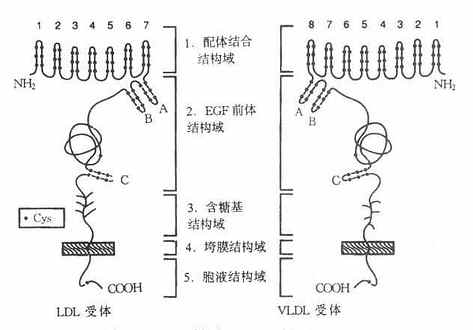
图4-6 LDL受体与VLDL受体结构示意图
1.配体结合结构域配体结合结构域由292个氨基酸残基组成,其中共有47个半胱氨酸(Cys)。含有七个由40个残基组成的与补体Cb和Cq类似的重复序列,每个重复系列中有6个半胱氨酸残基,所有42个半胱氨酸残基均已构成二硫键,重复序列2,3,6,7是结合LDL所必需,其中任何一种发生突变,均使受体丧失结合LDL的能力。重复序列5则与结合β-VLDL有关,若该序列突变时,受体结合β-VLDL的能力丧失60%。该受体不仅能结合LDL,还能结合VLDL、β-VLDL和VLDL残粒,它不仅能识别ApoB100,也可识别含ApoE的脂蛋白。ApoE、B100为LDL受体的配体,因此,LDL受体又称为ApoB100E受体。
2.EGF前体结构域该域约由400个氨基酸残基组成的肽段,有五个重复序列,每个重复序列包括25个氨基酸残基。EGF前体结构域与小鼠上皮细胞生长因子(epidermalgrowthfactor,EGF)前体有同源性,这一区域因此而得名。体外实验证实,这个区域的肽段,属于细胞膜外结构蛋白,起着支撑作用。
3.糖基结构域由58个氨基酸残基组成,是紧靠细胞膜面的肽段,有18个丝氨酸或苏氨酸,构成O-连接糖链,对LDL受体也有支撑作用。
4.跨膜结构由22个氨基酸残基组成,富含疏水氨基酸残基,属于跨膜蛋白,起着固系于细胞膜中的“抛锚”作用。这个区域若有缺陷则影响受体的细胞外分泌。
5.胞液结构域位于细胞膜的胞质侧,由50个氨基酸残基组成,C-末端位于胞质并“深埋”于胞质之中。
(二)LDL受体基因结构及功能
1.受体亲和性含ApoB100的脂蛋白可以与LDL受体以高亲和力结合,肠道分泌的ApoB48不是LDL受体的配体,所以肝脏不能清除完整的CM。
2.基因结构人LDL受体基因长度45ku,由18个外显子和17个内含子组成。
3.LDL受体途径LDL受体广泛分布于肝、动脉壁平滑肌细胞、肾上腺皮质细胞、血管内皮细胞、淋巴细胞、单核细胞和巨噬细胞,各组织或细胞分布的LDL受体活性差别很大。
LDL或其他含ApoB100、E的脂蛋白如VLDL、β-VLDL均可与LDL受体结合,内吞入细胞使其获得脂类,主要是胆固醇,这种代谢过程称为LDL受体途径(LDLreceptorpathway)。该途径依赖于LDL受体介导的细胞膜吞饮作用完成,如图4-7所示。当血浆中LDL与细胞膜上有被区域(coatedregion)的LDL受体结合(第1步),使其出现有被小窝(coatedpit)(第2步),并从膜上分离形成有被小泡(coatedvesicles)(第3步),其上的网格蛋白(clathrin)解聚脱落,再结合到膜上(第4步),其内的pH值降低,使受体与LDL解离(第5步),LDL受体重新回到膜上进行下一次循环(第6、7步)。有被小泡与溶酶体融合后,LDL经溶酶作用,胆固醇酯水解成游离胆固醇和脂肪酸,甘油三酯水解成脂肪酸,载脂蛋白B100水解成氨基酸。LDL被溶酶体水解形成的游离胆固醇再进入胞质的代谢库,供细胞膜等膜结构利用。胞内游离胆固醇在调节细胞胆固醇代谢上具有重要作用;若胞内浓度升高,可能出现下述种情况:①抑制HMGCoA还原酶,以减少自身的胆固醇合成;②抑制LDL受体基因的表达,减少LDL受体的合成,从而减少LDL的摄取,这种LDL受体减少的调节过程称为下调(downregulation);③激活内质网脂酰基CoA胆固醇酰转移酶(Acyl-CoAcholesterolacyltransferase,ACAT),使游离胆固醇在胞质内酯化成胆固醇酯贮存,以供细胞的需要。经上述三方面的变化,用以控制细胞内胆固醇含量处于正常动态平衡状态。血浆中胆固醇主要存在于LDL中,而65%-70%的LDL是依赖肝细胞的LDL受体清除。肝的LDL受体还影响LDL的合成速率及VLDL代谢。曾经认为人VLDL几乎全部在血循环中转变为LDL,LDL再被肝外组织摄取。现在经大鼠和兔实验研究表明,仅有15%以下转变为LDL,人则是小于50%的VLDL转变为LDL,大部分VLDL是以VLDL或VLDL残粒的形成被肝摄取。VLDL残粒与肝受体的亲和力比VLDL大很多。所以VLDL残粒被肝清除的速率比VLDL快。VLDL残粒大部分被肝清除,一小部分在肝脂酶作用下水解除去甘油三酯而转变成LDL。LDL受体还在乳糜微粒代谢中起一定作用。乳糜微粒中的ApoB48不能识别ApoB100E受体,所以肝不能清除完整的乳糜微粒。CM中虽有少量ApoE,因含有丰富的ApoC,可掩盖ApoE,而阻碍其与肝的ApoB、E受体结合,血液中乳糜微粒被脂蛋白脂肪酶水解去除其大部分甘油三酯核心后,同时丧失部分ApoC、A,生成乳糜微粒残粒后除去了阻碍ApoE与受体结合的因素,其残粒可迅速被肝清除,约有一半是通过LDL受体,另一半通过LDL受体相关蛋白代谢,其半寿期短。
总之,LDL受体主要功能是通过摄取Ch进入细胞内,用于细胞增殖和固醇类激素及胆汁酸盐的合成等。
二、VLDL受体
在ApoE100存在下,LDL受体可以结合LDL;有ApoE存在时,LDL受体既可结合LDL,又可结合VLDL、β-VLDL。与LDL受体不同,还有一种仅与含ApoE脂蛋白结合的特异受体存在,有以下临床现象及实验结果让人不得不推测还有另一种受体的存在:①纯合子FH患者血中乳糜微粒残粒并不增加;②LDL受体缺陷的WHHL兔乳糜微粒残粒仍正常地被肝摄取;③LDL受体下调状态下,乳糜微粒残粒可以在肝内异化,FH的LDL受体缺陷者或WHHL兔巨噬细胞不能利用LDL使之泡沫化,但可利用含ApoE脂蛋白的乳糜微粒残粒β-VLDL使其泡沫化,所以推测有对ApoE特异结合的另一种受体存在。
利用cDNA单克隆证明存在VLDL受体,其结构与LDL受体类似,如图4-6所示。由与LDL受体相同的五部分组成,即配体结合结构域、EGF前体结构域、含糖基结构域、跨膜结构域和胞液结构域。然而并非完全相同,配体域结构有32%的相同性,EGF前体结构域有52%的相同性;含糖基结构域仅有19%的相同性,跨膜域有32%相同性,胞质域有46%的相同性。LDL受体对含ApoB100的LDL,含ApoE的VLDL、β-VLDL、VLDL残粒有高亲和性。VLDL受体仅对含ApoE的脂蛋白VLDL、β-VLDL和VLDL残粒有高亲和性结合,并摄入细胞内,对LDL则为显著的低亲和性。VLDL受体在肝内几乎未发现,但是广泛分布在代谢活跃的心肌,骨骼肌、脂肪等组织细胞。
LDL受体受细胞内Ch(胆固醇,cholesterol)负反馈抑制,VLDL受体则不受其负反馈抑制。当VLDL受体的mRNA量成倍增加时,不受LDL乃至β-VLDL的影响。这是因为VLDL的配体关系使β-VLDL的摄取不受限制。这一点,对由单核细胞而来的巨噬细胞的泡沫化在早期动脉粥样硬化的斑块形成中有重要意义。
VLDL受体在脂肪细胞中多见,可能与肥胖成因有关。
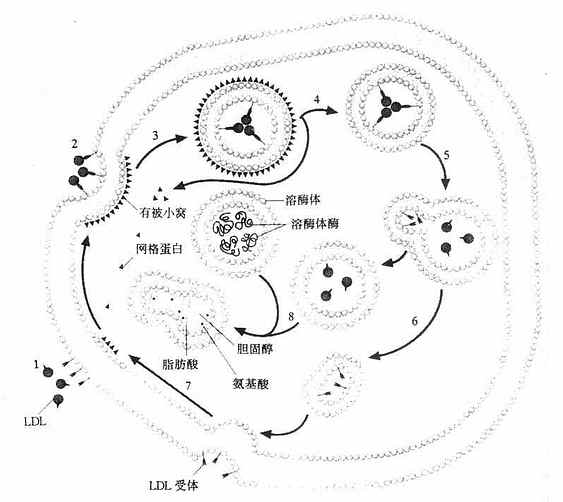
图4-7 LDL受体胞吞作用示意图
三、清道夫受体
遗传性的LDL受体缺陷的杂合子是不能摄取LDL的,但动脉粥样硬化斑块的巨噬细胞有从LDL来的胆固醇大量蓄积并泡沫化,其原因用LDL受体途径无法解释,因为从这条途径不可能摄取过多的脂质。Brown与Goldstein等使LDL乙酰化,从而导致不受细胞内胆固醇调节的过剩脂质也摄入,并出现异常蓄积,进而推测存在一种LDL受体途径以外的脂质摄取途径,使巨噬细胞摄取乙酰化LDL。Brown等人提出这种设想并定名为清道夫受体(scarengereceptor),以后许多实验证明了这种推测。其后,在细胞培养液中添加氧化剂使LDL氧化修饰,其结果使巨噬细胞摄取了这种变性LDL。现在认为,人体内脂质过氧化反应导致的变性LDL,可被巨噬细胞无限制地摄取入细胞内,这是因为变性LDL上带有各种分子的负电荷可与清道夫受体结合。
(一)清道夫受体结构
1990年用配体亲和层析和免疫亲和层析,将牛肺巨噬细胞清道夫受体纯化,并由其部分氨基酸序列克隆得到Ⅰ型、Ⅱ型清道夫受体cDNA。以后相继将人、兔和小鼠的清道夫受体cDNA克隆成功。该受体C-末端为半胱氨酸的为Ⅰ型,具有短肽结构的为Ⅱ型,清道夫受体共有两种亚基,以三聚体形式存在,是分子量为22万的膜糖蛋白;N末端在细胞膜内侧,C末端在膜外侧存在,是内翻外“inside-out”型的受体。该受体的Ⅰ、Ⅱ型均由六个区域部分组成,如图4-8所示。
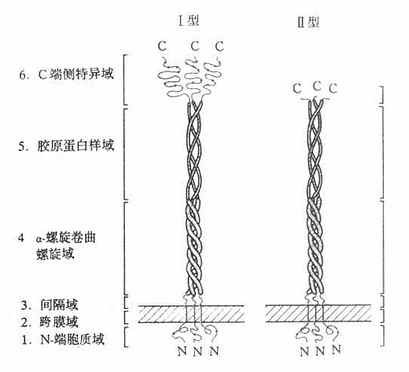
图4-8 清道夫受体结构示意图
1.N-端胞质域由50个氨基酸残基组成,可能与包涵素结合,类似LDL受体结构。其中央部分是磷酸化区域,是摄取配体的最重要的部位。
2.跨膜域(transmembrane)由第51-76氨基酸残基构成。为疏水性氨基酸组成的单一结构,“抛锚”固定于细胞膜上。
3.间隔域由第77-150氨基酸残基构成。
4.α-螺旋卷曲螺旋域(α-hericalcoiled-coil)由第151到271共121个氨基酸残基组成,此肽段常常先折叠成右手α-螺旋,每圈含3.5个氨基酸残基。这些α-螺旋又相互缠绕,构成平行的三股索状结构。这种右手螺旋索靠α-螺旋之间由脂肪族氨基酸的疏水核心来维持。
5.胶原蛋白样域属第273至343个氨基酸残基肽段,这种序列与胶原蛋白非常相似,推测这段肽链为右手胶原蛋白样三联体螺旋。
6.C-端侧特异域属第344至543个氨基酸残基肽段,为羧基末端,该段富含半胱氨酸。清道夫受体的8个半胱氨酸有6个在此范围,所以称为清道夫受体富含半胱氨酸域(scavengerreceptorcysteinrichdomainlike,srcR)。半胱氨酸的二硫键交联而成的区域非常紧密、牢固,形成球状,足以经受细胞外环境的影响,属于细胞外区域。
srcR域长约430nm,犹如三朵郁金香的“花苞”,由间隔域到α-螺旋卷曲螺旋域构成的“花茎”为支撑,这一“花茎”约占总长度的52%或胞外部分的62%。Ⅱ型清道夫受体没有srcR域,代之以6个氨基酸残基,所以是“截短”的清道夫受体,但Ⅱ型清道夫受体比Ⅰ型清道夫受体具有高亲和力结合和介导内移修饰LDL作用,配体谱很广。
(二)清道夫受体配体
清道夫受体配体谱广泛,有:①乙酰化或氧化等修饰的LDL;②多聚次黄嘌吟核苷酸,多聚鸟嘌吟核苷酸;③多糖如硫酸右旋糖酐;④某些磷脂,如丝氨酸磷脂,但卵磷脂不是配体;⑤细菌脂多糖,如内毒素等。这样广泛的配体谱的共同特点是多阴离子化合物。Ⅱ型清道夫受体没有srcR域,但仍具有与Ⅰ型相同的功能,显然配体结合域不在srcR域,推测其结合域在胶原蛋白样域,C末端的22个氨基酸残基作为配体识别位点,是结合多阴离子配体所必须的位点。
(三)清道夫受体功能
目前对于清道夫受体的功能还不十分清楚,是人们在研究巨噬细胞转变成泡沫细胞的机制时发现的。近年来大量实验证明LDL可被巨噬细胞、血管内皮细胞和平滑肌细胞氧化成氧化LDL,可通过清道夫受体被巨噬细胞摄骤,形成泡沫细胞。氧化LDL还能吸引单核细胞粘附于血管壁,对内皮细胞有毒性作用,从而促进粥样斑块形成。这些研究无疑阐明了巨噬细胞的清道夫受体在粥样斑块形成机制中起重要作用;另一方面,也推测巨噬细胞通过清道夫受体清除细胞外液中的修饰LDL,尤其是氧化LDL,是机体的一种防御功能。还有清除血管过多脂质,清除病菌毒素,摄取内毒素及其他多方面的功能。
清道夫受体分布于胎盘、肝、脾等单核吞噬细胞系统。
清道夫受体不仅在组织巨噬细胞内存在,在单核细胞分化由来的巨噬细胞侵入内皮下的过程中也见有该受体。兔、大鼠高脂肪膳食模型制作过程中,喂饲高胆固醇开始的几天见到LDL样粒子附着于血管壁,其后有单核细胞附着于内膜,巨噬细胞导致脂肪线条病巢形成,并以成百成千巨噬细胞簇出现,此时发现有大量的清道夫受体。当病灶逐步进入平滑肌细胞内膜后,其深部巨噬细胞仅有少量残存,受体量逐渐减少。若变性LDL显著增加时,清道夫受体摄取脂质的过程不受制约,可能这是脂质沉积的重要原因,也是动脉粥样硬化发病的重要机制。使LDL变性的主要因素是脂质的过氧化,然而是何种原因引起胆质过氧化的,尚待进一步研究。
-
《临床生物化学》 中的相关章节:
……
第三节 低血糖症
第四节 糖代谢的先天性异常
第四章 血浆蛋白及其代谢紊乱
第一节 血浆脂蛋白
第二节 载脂蛋白
第三节 脂蛋白受体(当前页)
第四节 脂代谢有关酶类与特殊蛋白质
第五节 脂蛋白代谢
第六节 脂蛋白代谢紊乱
第七节 脂蛋白代谢紊乱与动脉粥样硬化
……