第八节 细粒棘球绦虫
细粒棘球绦虫(Echinococus granulosus Batsch 1786)成虫寄生在犬科食肉动物,幼虫(称棘球蚴)寄生于人和多种食草类家畜,以及其它动物,引起一种严重的人兽共患病,称棘球蚴病或包虫病(echinococcosis,hydatid disease,hydatidosis)。棘球蚴病分布地域广泛。随着世界畜牧资源的开发而不断扩散,现已成为全球性的公共卫生问题。
形态
成虫是绦虫中最小的虫种之一,体长2~7mm,平均仅3.6mm。除头颈除外,整个虫体只有幼节、成节和孕节各一节,偶或多一节。头节略呈梨形,具有顶突和4个吸盘。顶突富含肌肉组织,伸缩力很强,其上有两圈大小相间的小钩共28~48个,呈放射状排列。顶突顶端有一群梭形细胞组成的顶突腺(rostellar gland),其分泌物可能具有抗原性。各节片均为扁长形。成节的结构与带绦虫相似,生殖孔位于节片一侧的中部偏后。睾丸45~65个,均匀地散布在生殖孔水平线前后方。孕节的生殖孔更靠后,子宫具不规则的分支和侧囊,含虫卵200~800个(图15-15)。
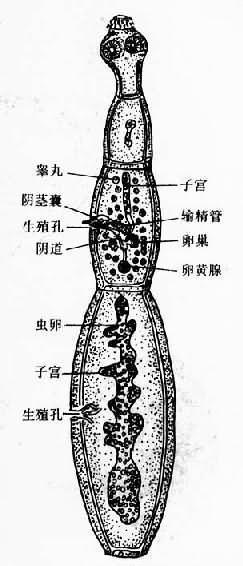
图15-15 细粒棘球绦虫成虫(采Nobel)
虫卵与猪、牛带绦虫卵基本相同,在光镜下难以区别。
幼虫即棘球蚴,为圆形囊状体,随寄生时间长短、寄生部位和宿主不同,直径可由不足1cm至数十厘米。棘球蚴为单房性囊,由囊壁和囊内含物(生发囊、原头蚴、囊液等)组成。有的还有子囊和孙囊。囊壁外有宿主的纤维组织包绕(图15-16)。
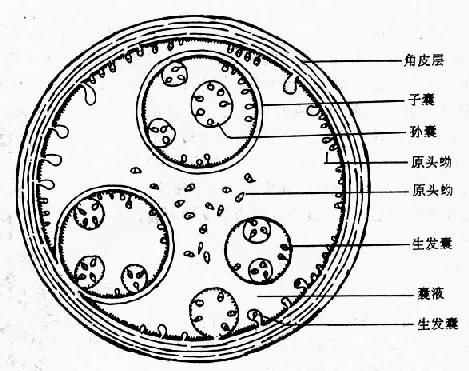
图15-16 棘球蚴
囊壁分两层,外层为角皮层(laminated layer),厚约1mm,乳白色、半透明,似粉皮状,较松脆,易破裂。光镜下无细胞结构而呈多层纹理状。内层为生发层(germinal layer)亦称胚层,厚约20µm,具有细胞核。生发层紧贴在角皮层内,电镜下可见从生发层上有无数微毛延伸至角皮层内。囊腔内充满囊液,亦称棘球蚴液(hydatid fluid)。囊液无色透明或微带黄色,比重1.01~1.02,pH6.7~7.8,内含多种蛋白、肌醇、卵磷脂、尿素及少量糖、无机盐和酶,对人体有抗原性。
生发层(胚层)向囊内长出许多原头蚴(protoscolex),原头蚴椭圆形或圆形,大小为170×122µm,为向内翻卷收缩的头节,其顶突和吸盘内陷,保护着数十个小钩。此外,还可见石灰小体等。原头蚴与成虫头节的区别在于其体积小和缺顶突腺(图15-17)。
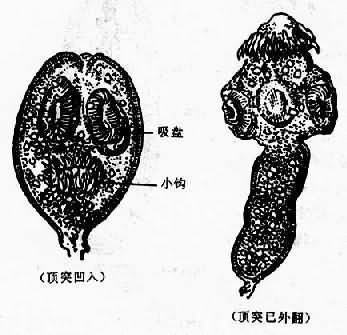
图15-17 细粒棘球绦虫原头蚴
生发囊(brood capsule)也称为育囊,是具有一层生发层的小囊,直径约1cm,由生发层的有核细胞发育而来,据丁兆勋等观察,最初由生发层向囊内芽生成群的细胞,这些细胞空腔化后,形成小囊并长出小蒂与胚层连接。在小囊壁上生成数量不等的原头蚴,多者可达30~40个(图15-18)。原头蚴可向生发囊内生长,也可向囊外生长为外生性原头蚴。
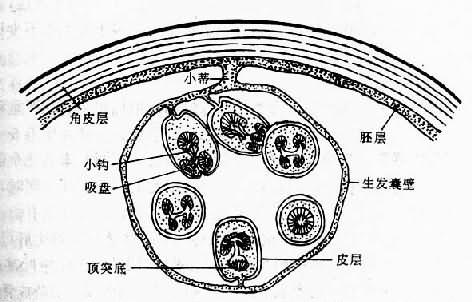
图15-18 棘球蚴及生发囊模式图(仿Morseth)
子囊(daughter cyst)可由母囊(棘状蚴囊)的生发层直接长出,也可由原头蚴或生发囊进一步发育而成。子囊结构与母囊相似,其囊壁具有角皮层和生发层,囊内也可生长原头蚴、生发囊、以及与子囊结构相似的小囊,称为孙囊(grand daughter cyst)。有的母囊无原头蚴、生发囊等,称为不育囊(infertile cyst)。
原头蚴、生发囊和子囊可从胚层上脱落,悬浮在囊液中,称为囊砂或棘球蚴砂(hydatid sand)。
生活史
细粒棘球绦虫的终宿主是犬、狼和豺等食肉动物;中间宿主是羊、牛、骆驼、猪和鹿等偶蹄类,偶可感染马、袋鼠,某些啮齿类、灵长类和人。
成虫寄生在终宿主小肠上段,以顶突上的小钩和吸盘固着在肠绒毛基部隐窝内、孕节或虫卵随宿主粪便排出。孕节有较强的活动能力,可沿草地或植物蠕动爬行,致使虫卵污染动物皮毛和周围环境,包括牧场、畜舍、蔬菜、土壤及水源等。当中间宿主吞食了虫卵和孕节后,六钩蚴在其肠内孵出,然后钻入肠壁,经血循环至肝、肺等器官,经3~5个月发育成直径为1~3cm的棘球蚴。随棘球蚴囊大小和发育程度不同、囊内原头蚴可由数千至数万,甚至数百万个。原头蚴在中间宿主体内播散可形成新的棘球蚴,在终宿主体内可发育为成虫(图15-19)。
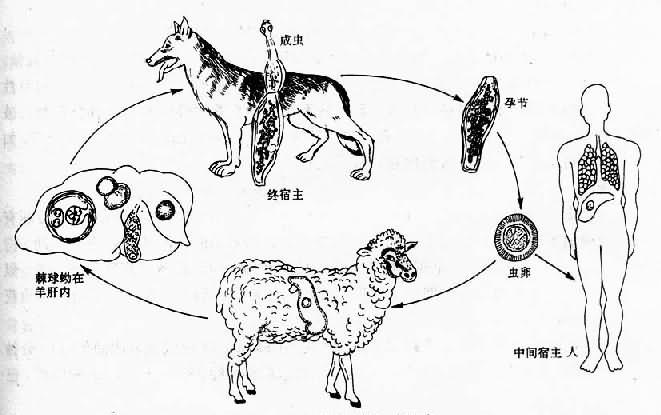
图15-19 细粒棘球绦虫生活史
棘球蚴被犬、狼等终宿主吞食后,其所含的每个原头蚴都可发育为一条成虫。故犬、狼肠内寄生的成虫也可达数千至上万条。从感染至发育成熟排出虫卵和孕节约需8周时间。大多数成虫寿命约5~6个月。
人可作为细粒棘球绦虫的中间宿主。当人误食到虫卵后,六钩蚴即经肠壁随血循环侵入组织,引起急性炎症反应单核细胞浸润,若幼虫未被杀,则逐渐形成一个纤维性外囊,在内缓慢地发育成棘球蚴。故棘球蚴与宿主间有纤维被膜分隔。一般感染半年后囊的直径达0.5~1.0cm,以后每年增长1~5cm,最大可长到数十cm。棘球蚴在人体内可存活40年甚至更久。但如遇继发其它感染或外伤时,可发生变性衰亡,囊液浑浊而终被吸收和钙化。
棘球蚴在人体内可发现于几乎所有部位。据我国新疆15298例病人分析,最多见的部位是肝(占69.9%),多在右叶,肺(19.3%)次之;此外是腹腔(3%)、以及原发在肝再向各器官转移(5.3%),其他部位分别是:脑(0.4%)、脾(0.4%)、盆腔(0.3%)、肾(0.3%)、胸腔(0.2%)、骨(0.2%)、肌肉(0.1%)、胆囊(0.1%)、子宫(0.1%)以及皮肤、眼、卵巢、膀胱、乳房、甲状腺等(0.4%)。在肺和脾内棘球蚴生长较快。在骨组织内则生长极慢。巨大的棘球蚴囊多见于腹腔,它可以占满整个腹腔,推压膈肌,甚至使一侧肺叶萎缩。棘球蚴在人体内一般为单个寄生,但多个寄生也不少见,约占患者的20%以上。
致病
棘球蚴对人体的危害以机械损害为主。棘球蚴病,俗称包虫病,严重程度取决于棘球蚴的体积、数量、寄生时间和部位。因棘球蚴生长缓慢,往往在感染5~20年才出现症状,原发的棘球蚴感染多为单个;继发感染常为多发,可同时累及几个器官。由于棘球蚴的不断生长,压迫周围组织、器官,引起组织细胞萎缩、坏死。同时,因棘球蚴液渗出或溢出可引起毒性或过敏性反应。临床表现极其复杂,常见症状有:
1.局部压迫和刺激症状 受累部位有轻微疼痛和坠胀感。如寄生肝可有肝区疼痛,在肺可出现呼吸急促、胸痛等呼吸道刺激症状,在颅脑则引起头痛、呕吐甚至癫痫等,骨棘球蚴常发生于骨盆、椎体的中心和长骨的干骺端、可破坏骨质,易造成骨折或骨碎裂。
2.包块 位置表浅的棘球蚴可在体表形成包块,触之坚韧,压之有弹性,扣诊时可有棘球蚴震颤。
3.过敏症状 常有荨麻疹、血管神经性水肿和过敏性休克等。
4.中毒和胃肠功能紊乱 如食欲减退、体重减轻、消瘦、发育障碍和恶病质现象。
一旦棘球蚴囊破裂,可造成继发性感染。如肝棘球蚴囊破裂可进入胆道,引起急性炎症,出现胆绞痛、寒战高热黄疸等。破入腹腔可致急性弥漫性腹膜炎。肺棘球蚴如破裂至支气管,可咳出小的生发囊、子囊和角皮碎片。囊液大量溢出可产生过敏反应,如进入血循环可引起严重的过敏性休克,甚至死亡。
诊断
询问病史,了解病人是否来自流行区,以及与犬、羊等动物和皮毛接触史对诊断有一定参考价值。X线、B超、CT及同位素扫描等对棘球蚴病的诊断和定位也有帮助。特别是CT,不仅可早期诊断出无症状的带虫者,且能准确地检测出各种病理形态影像。但确诊应以病原学结果为依据,即手术取出棘球蚴,或从痰、胸膜积液、腹水或尿等检获棘球蚴碎片或原头蚴等。
免疫学试验是重要的辅助诊断方法。卡松尼(Casoni)皮内试验方法简便,15分钟即可得出结果,阳性率78.6%~100%,但易出现假阳性(约18%~67%)或假阳性,已渐少用。
常用的血清学检查法有酶联免疫吸附试验(ELISA)、对流免疫电泳(CIEP)和间接血凝试验(IHA),均较敏感;间接荧光抗体试验(IFA)、胶乳凝集试验(LAT)和水化矽酸铝絮状试验则次之。目前以亲和素-生物素-酶复合物酶联免疫吸附试验(ABC-ELISA)敏感性最高,比常规ELISA高4~6倍,而且假阳性很少。斑点酶联免疫吸附试验(Dot-ELISA)则因操作简便、观察容易,很适于基层使用。目前认为对包虫病的免疫诊断应采取综合方法,经皮内试验过筛阳性者,应再加2~3项血清学试验以提高诊断准确率。
流行
细粒棘球绦虫有较广泛的宿主适应性,但很自然环境和人的生产活动影响,其终宿主和中间宿主动物长期形成了比较固定的动物间循环关系,绦虫也因此通过突变,形成了两大遗传侏系:①森林型,流行细粒棘绦虫北方株。受北极和全北区地理景观条件影响,主要在犬、狼和鹿之间形成野生动物循环。②畜牧型,流行细粒棘球绦虫欧洲株。受人生产活动影响,分布遍及世界各大洲牧区,主要以犬和偶蹄类家畜之间循环为特点。畜牧型中,又有羊/犬、牛/犬和猪/犬等不同类型。在我国分布较广的是绵羊/犬动物循环。其次是牦牛/犬循环,仅见于青藏高原和甘肃省的高山草甸和山麓地带。
我国的细粒棘球绦虫和棘球蚴病主要流行在西北广大农牧区,即新疆、青海、甘肃、宁夏、西藏和内蒙6省、区,其次是陕西、河北、山西和四川四部;另外在东北三省、河南、山东、安徽、湖北、贵州和云南等省有散发病例。迄今全国已有23个省、市、区证实有当地感染病人。
在西北5省区流行区,据近年普查,人群患病率在0.6%~4.5%之间,主要动物中间宿主绵羊的棘球蚴感染率在3.3%~90%之间,家犬的成虫感染率在7%~71%之间,人群中最易感染者是学龄前儿童(新疆15298例病人中,15岁以下者占32.1%)。流行严重的因素主要有以下3点:
1.虫卵对环境的严重污染 牧区犬感染通常较重,使犬粪中虫卵量很大,随动物的活动以及尘土、风、水等播散,导致虫卵严重污染环境。虫卵对外界低温、干燥及化学药品有很强抵抗力。在2℃水中能活2.5年,在冰中可活4个月,经过严冬(-12~-14℃仍保持感染力。一般化学消毒剂不能杀死虫卵。
2.人与家畜和环境的密切接触 牧区儿童多喜欢与家犬亲昵,很易受到感染,成人感染可因从事剪羊毛、挤奶、加工皮毛等引起;许多人则通过食入被虫卵污染的水、蔬菜或其它食物而受染。
3.病畜内脏喂狗或乱抛 在大量的家庭分散宰屠中,因缺乏卫生知识,常以病畜内脏喂狗,或将其随地乱抛,脏器内的棘球蚴和原头蚴在外界,特别在低温时能存活较久,如在20~22℃能活2天、10~15℃4天,-2~2℃可活10天,因此能使野犬、狼、豺受到感染。反过来又加重羊、牛感染,使流行愈趋严重。
在非流行区人因偶尔接触受感染的犬,或接触到来自流行区的动物皮毛而受感染。随着我国经济迅速发展,流行区的畜产品大量流向内地,各地也不断开辟新的牧场和草场,引起和饲养大批牲畜,可形成新的污染地带。因此,潜在的流行危险日益严重。我国已成为世界上人、畜棘球蚴病最严重的国家之一。
防治原则
在流行区应采取综合性预防措施,主要包括以下几方面:
1.加强宣传,普及棘球蚴病知识,提高全民的防病意识,在生产和生活中加强个人防护,杜绝虫卵感染。
2.结合必要的法规强化人的卫生行为规范,主要是根除以病畜内脏喂犬和乱抛的陋习;加强对屠宰场和个体屠宰的检疫,及时处理病畜内脏。
3.定期为家犬、牧犬驱虫,捕杀牧场周围野生食肉动物。我国卫生部1992年颁布了新的全国包虫病防治规划,在流行区推行以健康教育、屠宰卫生管理和家犬管理以及药物驱虫为主的综合防治措施。经过几年实施,现正取得效果。
棘球蚴病的治疗,首选方法是外科手术,术中应注意务将虫囊取尽并避免囊液外溢造成过敏性休克或继发性腹腔感染。近年来推广的内囊摘除术和新的残腔处理办法已使手术治愈率明显提高。对早期的小棘球蚴,可使用药物治疗,目前以丙硫咪唑疗效最佳,亦可使用吡喹酮、甲苯咪唑等。
-
《人体寄生虫学》 中的相关章节:
……
第三节 阔节裂头绦虫
第四节 链状带绦虫
第五节 肥胖带绦
第六节 微小膜壳绦虫
第七节 缩小膜壳绦虫
第八节 细粒棘球绦虫(当前页)
第九节 多房棘球绦虫
第十节 犬复孔绦虫
第十一节 其它人体寄生绦虫
第十六章 线虫
……